
5月4日,百泰克生物的一次性使用病毒采样管取得美国FDA 510K注册批件,成为该类产品首个获此国际权威认证的中国企业。
510K是美国食品药品管理局(FDA)针对所有拟进入美国市场销售的医疗器械产品进行注册认证审核所遵循的基础法规,位于FD&C Act第510章节,由于相当完善齐全、在全世界非常具有权威性而著称。

据悉,百泰克该项认证历时两年;2020年9月,该产品以其优异的保存性能和超群的检测灵敏度,率先成为美国FDA紧急授权使用的两家中国厂商之首,并先后获得欧盟CE认证、英国MHRA注册、加拿大MDEL、巴西、沙特、澳大利亚、加拿大、意大利、马来西亚和印度尼西亚等15个国家和地区的认证。



百泰克病毒采样管海外使用场景
一次性使用病毒采样管广泛用于临床新冠病毒、流感、禽流感、手足口病、麻疹等病毒样本的采集及转运保存,对拭子进行不同的处理,搭配不同的运输介质,可构成不同类型样本的收集与运输组件,应用于不同场景。在整个采样组件中,保存液对于样本的保存效果是检验产品性能的重要指标,保存温度、时长都将成为影响保存效果的因素。经对国产主流采样管保存效果的比对测试,检测在室温、不同保存时间(第一天、第三天、第七天)条件下新冠病毒的核酸检测灵敏度;结果显示,百泰克的一次性使用病毒保存管ITM、VTM、UTM系列的Ct值均比市场上常见品牌保存管的更低,检测灵敏度更高,1-7天内Ct值差异较小,保存效果更为稳定。
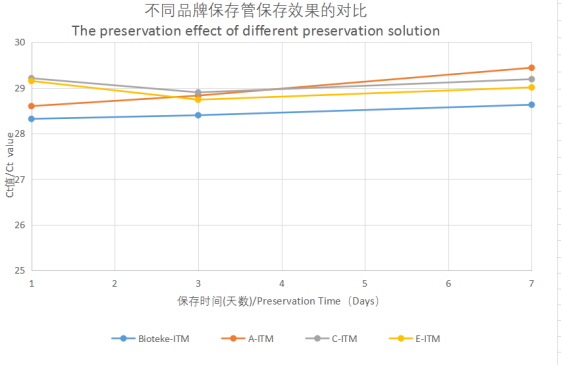
百泰克灭活保存液(ITM)系列与其他品牌保存效果对比
无锡百泰克生物技术有限公司成立于2010年8月,2017年入驻惠山生命园,主要从事体外诊断试剂仪器的研发、生产及销售等,在北京、深圳、无锡、上海、苏州和泰州等地建有生产基地和研发中心。公司产品包含一次性使用病毒采样管、核酸采样拭子、全自动核酸提取仪、核酸提取试剂、新冠病毒抗原检测卡、荧光定量PCR仪等核酸提取纯化及检测设备以及消毒系列等,覆盖科研、临床、诊断等领域。主要产品已通过数十项CE认证、FDA认证,获多个国家和地区的注册证;全自动核酸提取仪、核酸气溶胶污染清除仪入选省重点推广应用的新技术新产品目录。公司先后通过无锡市“瞪羚”企业遴选、获市专精特新“小巨人”企业、市企业技术中心、市工程技术研究中心等荣誉,并主持省重点研发计划等科技计划5项。